



对于固态科学家来说,无法获得先前制备的晶型是一个令人沮丧且有很大潜在风险的情况。这篇综述对多晶型物消失的案例进行讨论,以证明消失的多晶型现象在固态研究中持久的相关性。
01 简介
想要得到最稳定的晶型,通常需要设置数百次或数千次的结晶筛选实验。然而,新晶型可能会在筛选实验完成很久之后突然出现。这种新出现的晶型可能表现出完全不同的固态性质,新晶型可能在化合物开发的后期阶段甚至产品上市后出现。与此同时,根据Ostwald's规则,热力学上更稳定的晶型出现后,已知的较不稳定的晶型会消失,这代表着整个生产过程的失控。虽然这会在目标化合物开发过程甚至上市产品的固态形式确认中造成麻烦,但新晶型的出现,不一定完全带来负面的影响,也可能会带来更优的理化性质。
然而,目前对晶体成核和生长机制的理解,仍然不足以精确控制多晶型(或任何其他晶型)的形成或消失。在30 年前的一篇综述中,表达了晶体形式不会永远消失的观点;一旦已经获得了某一个晶型,原则上在满足正确实验条件的情况下,出现的晶型是可以重复制备的。
02 消失的多晶型——概念和误解
2.1 概念
消失的多晶型指的是至少被成功制备过一次,并且通过某些观察或测试证实其存在过的晶型。随后尝试通过相同方法重复制备该晶型时,却得到了不同的晶型,要么单独出现,要么与旧晶型一起出现成为混晶。如果首次重复制备中出现的就是混晶,那么在随后的制备中,新晶型通常会占据主导地位,而旧晶型则不再出现。
每次结晶都是动力学和热力学因素之间的竞争。只要找到合适的实验条件,总是有可能再次获得[旧晶型]——热力学和动力学条件。
重新获得一种已经消失的晶型可能需要相当多的时间和精力,并需要一些富有创造性的化学方法。下面给出的例子将展示用于重新获得消失晶型的各种策略。
2.2 晶种和加晶种
加晶种是一种在制药行业被广泛应用的诱导结晶技术。晶种的无意引入则是由于存在足够少量(原则上一个颗粒就足够)的晶体。晶种的无意引入经常被用来解释那些难以解释晶型消失现象。尽管关于这些晶种的大小和活性范围尚未达成共识,且这些晶种实际上从未被直接观察到。
结晶作为最经典的纯化方法,是在本科有机化学实验教材的纯化方法中最早被提及的纯化方法之一。晶种的存在,可以用来解释一种晶型消失而另一种新晶型出现的现象。新晶型晶种的出现可能非常具有侵略性,阻止了旧晶型的结晶。然而,并没有内在的原因说明每个系统都会受到这种新晶种出现的影响。有许多已知的多晶型案例,其中各种晶型可以在已知其他晶型存在的情况下制备和维持。常规的多晶型,每个晶型系统都是独特的,必须单独研究和表征,以了解如何制备和表征。
03 多晶型消失案例
本节描述了几个著名的多晶型消失的案例。
3.1 盐酸雷尼替丁
在20世纪70年代初,James Black在(当时的)Smith, Kline & French公司发现了组胺2型(H2)受体,并通过制备一系列H2受体拮抗剂开发了第一种抗溃疡药物西咪替丁(Tagamet),为此他获得了1988年诺贝尔医学奖。H2受体拮抗剂是20世纪的奇迹药物之一。在它们问世之前(以及随后的质子泵抑制剂的出现),全球有数百万的消化性溃疡患者,其中相当一部分人因此丧生;自从这些药物问世以来,现代医学院的课程中基本上已经不再教授切除消化性溃疡的手术程序。
西咪替丁的巨大成功引发了全行业开发更多H2受体拮抗剂的努力。1977年,Allen & Hanbury(当时是葛兰素集团研究的一部分,现为GSK)开发了雷尼替丁及其盐酸盐(图1a),并于1978年获得了美国专利。在雷尼替丁碱的多步合成后制备其盐酸盐的方法在专利的“实施例32”中给出(图1b)。
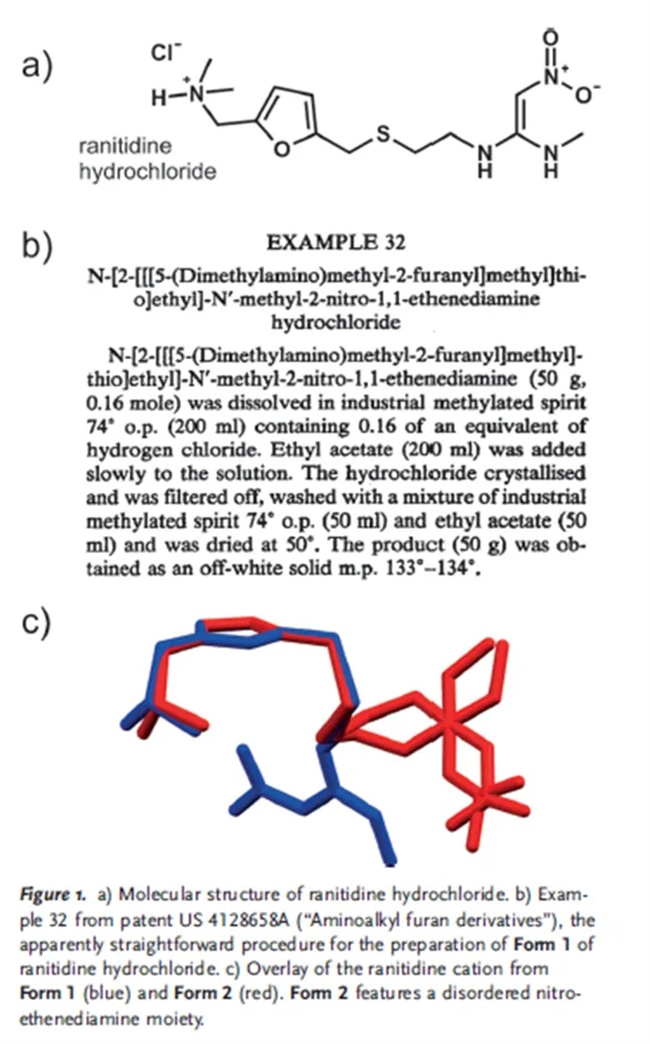
在随后的近四年时间里,药物的开发涉及在公司中试工厂中通过基本采用实施例32中描述的化学方法进行批量放大至多公斤规模。1980年4月15日制备的批次未能通过红外,在1045 cm−1处显示了一个未观察到的尖锐峰,表明形成了一种新的晶型,命名为Form 2。随后的四个批次显示出Form 2的含量逐渐增加,而相同的工艺不再产生(现在命名的)Form 1。通过基本相同的工艺恢复生产Form 1的多次尝试均未成功。因此,这显然是一个消失的多晶型案例。偶然的是,Form 2具有显著改善的过滤和干燥特性,这些特性加上新晶型的新颖性,构成了1985年获批的专利申请的基础。两种晶型的晶体结构随后被确定;两种晶型均在单斜晶系P21/n空间群中结晶,其中雷尼替丁阳离子的硝基乙烯二胺部分显示出不同的构象和无序程度(图1c)。因此,这也是一个构象多晶型的例子。
葛兰素(Glaxo)于1984年推出了盐酸雷尼替丁,商品名为Zantac®,到1992年,它成为全球最畅销的药物,年销售额达到34.4亿美元,而当时第二大药物(拜耳的Adalat Procardia®)的销售额约为其一半。
到1990年,许多仿制药公司计划在Form 1专利于1995年到期后进入市场。制备Form 1的尝试基于执行实施例32。正如在随后的诉讼过程中所揭示的,这些尝试基本上都是从商业化的Form 2开始的。
在根据实施例32多次尝试制备Form 1后,加拿大仿制药公司Novopharm几乎全部得到了Form 2,他们称葛兰素从未制备过Form 1,并寻求FDA批准销售Form 2。葛兰素试图通过起诉Novopharm(及其他公司)侵犯其Form 2专利来阻止他们进入市场。Novopharm承认侵犯了Form 2专利,但辩称Form 2专利在Form 1专利中已被披露,因为他们根据实施例32尝试制备Form 1时得到了Form 2。Novopharm认为支持Form 1专利的实验过程存在缺陷,葛兰素则回应称对方的实验被晶种污染,因此未能再现实施例32。
美国法律中的概念要求的是实验过程的一致性结果,即必须是不变或可变的。因此,为了支持其反对固有预期的案件,葛兰素原则上必须证明实施例32并不必然或总是产生Form 2,而是实际上可以产生Form 1。
为此,在1993年8月的审判过程中,首次制备盐酸雷尼替丁的实验记录被审查、交叉审查,并与实施例32的措辞进行了比较。该记录本中包含了三个不同的实施例。记录本中的实验文本并非逐字相同,也没有一个与实施例32的语言完全相同,关于这些差异固态研究专业人员进行了大量讨论。此外,牛津大学的Sir Jack Baldwin,在1993年让他的两位资深博士后研究员根据Form 1专利完成了雷尼替丁碱的整个合成,然后使用该碱重现了实施例32。他们也三次获得了Form 1。
根据实施例32制备Form 1的这六个实例足以克服固有性的论点。Form 2专利被认定为有效,Novopharm(及其他公司)在2002年专利到期之前被限制销售Form 2。
3.2 利托那韦
最著名的消失多晶型案例是利托那韦(图2a),这是一种抗病毒化合物,由雅培实验室于1996年以Norvir™的名义上市,以半固体凝胶胶囊的形式用于治疗获得性免疫缺陷综合征(艾滋病)。这些胶囊基于开发过程中发现的唯一已知晶型Form I。然而,在1998年,一种新的、溶解度显著降低的利托那韦多晶型意外地在半固体凝胶胶囊中沉淀出来,从而导致胶囊的溶出度测试失败。随后的研究表明,这种新晶型(称为Form II)在醇水溶液中的溶解度显著低于市售的Form I。此外,研究发现,Form II使得任何引入Form II的实验室都无法再获得Form I。由于这事件,利托那韦不得不暂时从市场上撤出。
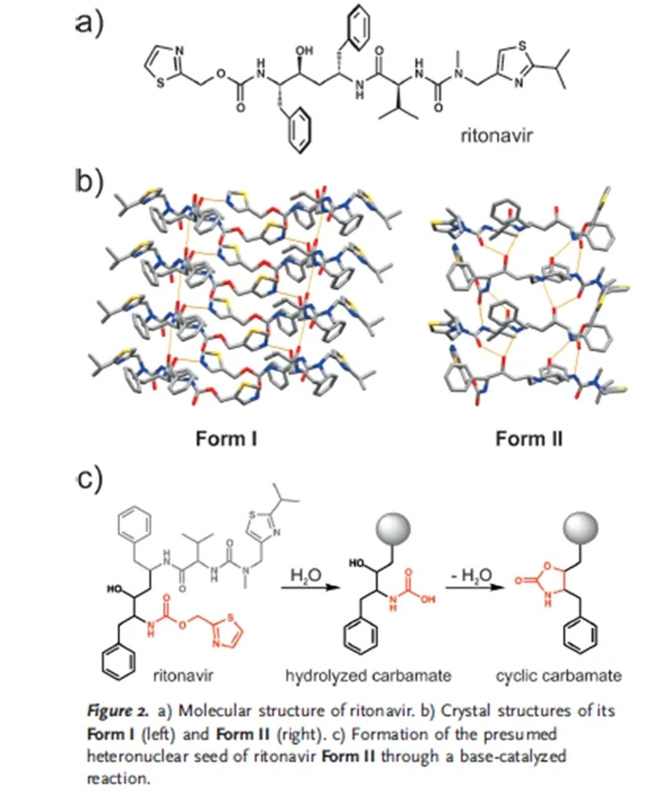
晶体学分析表明,Form I的晶体结构以类似于β-折叠结构的利托那韦堆叠为特征(图2b)。另一方面,Form II的晶体结构由强氢键连接的一维利托那韦堆叠组成(图2b)。 Form I的较高晶体密度表明它也是更稳定的晶型。 此外,对剑桥结构数据库(CSD)进行检索,Form I利托那韦的氨基甲酸酯部分表现出统计上更有利的构象。该分析与溶液中的NMR研究一致,该研究揭示了溶液中存在两种构象异构体,比例约为99:1。这些构象异构体不能明确地解析为Form I和Form II,但注意到观察到的99:1比例与最初发现的单一多晶型(即Form I)一致。Form II的较高稳定性最终归因于氢键模式的形成,其中与Form I不同,“所有强氢键供体和受体都得到了满足”。这一论点与Form II具有较高熔点和熔化热(约125°C,87.8 J g−1−1)而Form I(约122°C,78.2 J g−1−1)的观察结果一致。
研究发现利托那韦在碱催化反应中降解,形成一种带有氨基甲酸酯的产物(图2c),其结构与Form II中利托那韦的构象相关。还发现降解产物形成非常迅速,并且由于其更高的稳定性,其溶解度低于利托那韦。结论是,降解产物可能从经历了溶剂损失的利托那韦溶液中结晶出来,然后作为Form II的晶种。
最终研究表明,在受控条件下,在曾经接触过Form II的实验室中可以实现Form I的结晶。利托那韦最终在1999年重新申请并获得批准,随后重新上市。据估计,公司因此损失了超过2.5亿美元的收入。
后期尝试对利托那韦进行进一步高通量多晶型筛选,以全面探索该化合物的多晶型。该筛选包括约2000个结晶实验,结果除了Form I和Form II外,还发现了三种新的晶型——即一种亚稳态多晶型、一种三水合物和一种甲酰胺溶剂化物。这些发现突出了利用多种结晶方法的必要性,特别是在这种情况下,高通量筛选与精心设计的结晶实验相结合,以检索与分子结构景观相关的结构。
3.3 盐酸帕罗西汀
盐酸帕罗西汀是一种用于治疗抑郁症的血清素再摄取抑制剂。化合物帕罗西汀最初由丹麦公司Ferrosan在20世纪70年代开发。Beecham(现为葛兰素史克GSK的一部分)于1980年购买了帕罗西汀的权益,并开发盐酸帕罗西汀。Beecham开发了一种生产结晶形式盐酸帕罗西汀的工艺,后来被称为“无水物”结晶形式。然而,在1984年末,在中试工厂放大过程中,相隔仅几周“半水合物”结晶形式突然在英国的两个Beecham工厂中相继出现。新的半水合物形式被命名为Form 1,而之前存在的无水物被标记为Form 2(图3)。
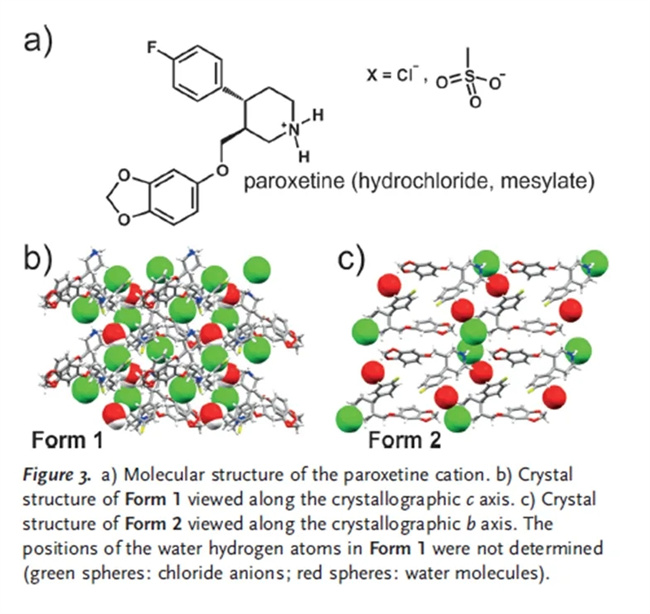
半水合物不吸湿,并且表现出比无水物更优越的物理性质。1986年,GSK在美国申请了半水合物的专利,并于1988年获得批准。酸帕罗西汀最终于1993年以半水合物形式上市,商品名为Paxil®。
在20世纪80年代, Beecham进一步研究了无水物和半水合物的性质。结果表明,在存在水(或湿度)的情况下,无水物会转化为半水合物,这一过程在温度、压力和半水合物晶种的作用下会加速。因此,在存在水或湿度的环境中,且存在半水合物晶种时,很难避免无水物向半水合物的转化。
1998年,加拿大仿制药制造商Apotex向FDA提交了一份仿制药上市申请(ANDA),以销售已过专利期的无水盐酸帕罗西汀(Form 2)的仿制药。半水合物专利于2006年到期。根据《Hatch-Waxman法案》的条款,GSK反对Apotex的申请,认为无水形式(Form 2)会转化为半水合物(Form 1)。GSK的论点部分基于证据,即Apotex在开发其无水产品时,将半水合物带入了其生产设施,从而提供了已被证明是转化因素的晶种。此外,在API的制造、制剂以及最终药丸的水基包衣过程中都接触到了水,并且在最后加工步骤中使用了压力。Apotex的许多无水物批次已经表现出晶型转化现象,有些批次的无水物在40°C/75%湿度下储存一个月后几乎完全转化为半水合物。此外,Apotex对物料的放行基于比较光谱数据的方法,该方法无法检测到API中少于5-8%的侵权半水合物。
法官驳回了Apotex关于晶种的论点,称“认为晶种发生没有科学依据……显然是错误的。” 在他的裁决中,他发现Apotex的无水物会转化为半水合物,并且“可能会持续到达到100%。” 他还发现Apotex在所谓的无水材料中对半水合物的检测限为5-8%,但在确定Apotex是否侵犯GSK专利时,法官最终仍裁定支持Apotex。
后来Pina等人证明,最初被描述为吸湿性无水物的Form 2实际上是一种非化学计量的水合物,尽管晶格中没有连续的通道,但它非常容易脱水和再吸水。Form 1的较高稳定性归因于晶格中保留了更多的氢键来固定水分子。
3.4 帕罗西汀甲磺酸盐(帕罗西汀甲磺酸酯)
盐酸帕罗西汀的市场成功(2001年全球销售额达32亿美元)促使许多制药公司寻找其他晶型。一种方法是制备不同的盐。20世纪90年代中期,英国的SmithKline Beecham(现为GSK)和荷兰的Synthon独立成功制备了帕罗西汀的甲磺酸盐(甲磺酸酯)。考虑到化学性质,两项专利中的盐化学性质的相似并不令人惊讶。第一项美国专利于1999年2月23日授予Synthon。另一项美国专利在近15个月后的2000年5月16日授予SmithKline Beecham。
为什么可以为同一种盐颁发两项专利?一个明显的可能性是它们是同一种盐的两种不同晶型,这应该可以从专利中提供的分析数据中辨别出来。表1包含了两项专利中相关数据的比较。显然,唯一可以比较的数据是来自红外光谱的数据。两项专利中的红外数据见表2。两个峰值列表的比较表明它们并不是相同的晶型。在诉讼过程中,很明显,自Synthon专利发布以来,每次报告的帕罗西汀甲磺酸盐合成都产生了SmithKline Beecham专利中发现的峰值。这种情况只有两种解释:1)Synthon晶型是一种消失的多晶型,至少被制备和表征过一次,随后的制备和结晶导致了SmithKline Beecham晶型,或2)Synthon数据有误。
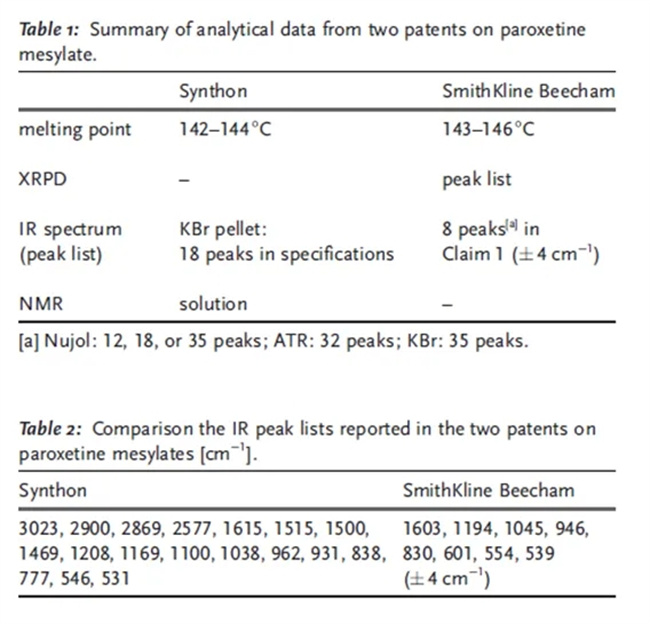
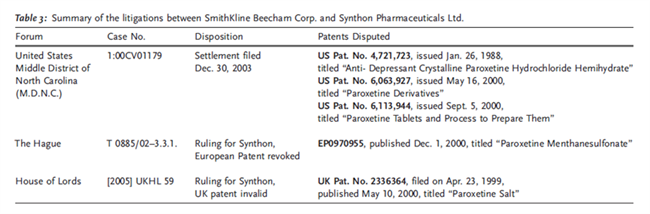
关于这两项专利(及其欧洲等效专利)中报告的帕罗西汀甲磺酸盐问题的系列诉讼未能就该问题达成法律共识。表3总结了其中一些诉讼。
尽管文献中未报道,帕罗西汀甲磺酸盐案例是一个突出的例子,强调了彻底研究、表征和记录API和特种化学品的必要性。
3.5 罗替高汀
罗替高汀(图4a)是一种非麦角衍生的多巴胺激动剂,用于治疗帕金森病。它由UCB以Neupro®的名称销售,并通过透皮贴剂给药,以尽量减少药物的不良副作用。
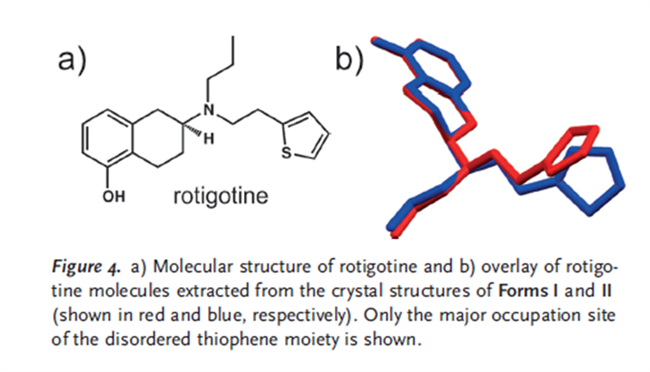
Neupro®于2007年获得欧洲药品管理局(EMEA)批准在欧洲使用,随后获得FDA批准进入美国市场。2008年,Neupro®贴剂中出现了一种以前未知且热力学更稳定的多晶型,表现为“雪状晶体”。这种新的多晶型是未预料到的,因为该药物自20世纪80年代就已确立,且在药物开发期间或之后未观察到多晶型现象。虽然新的多晶型(Form II)在疗效上没有降低,但建议医生、分销商、药剂师和患者冷藏他们的Neupro®库存,因为冷藏储存显著降低了结晶速率。UCB继续在欧洲供应Neupro®,但特定批次被召回,并由制造后立即冷藏的批次替换。在FDA建议重新配制药物后,UCB的新Neupro®配方于2012年获得批准,该配方不需要冷藏。
罗替高汀更稳定的Form II的起源尚不清楚,但可以合理推测,多晶型转变是由贴剂或药物本身中的某个事件或杂质突然触发的。Form II密度更高(因此根据Burger-Ramberger密度规则可能更稳定),并且伴随着由噻吩和烷基部分之间的扭转角调整引起的构象变化。
3.6 DMP543
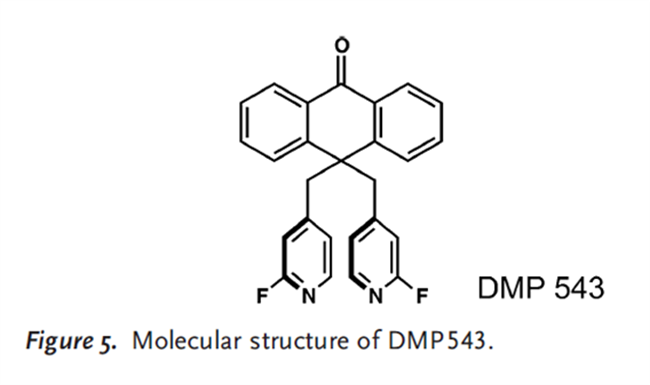
杜邦公司在20世纪80年代开发了一种有效、血浆持续时间长和脑渗透特性强的乙酰胆碱释放增强剂——DMP543(图5)。在药物开发的早期阶段,DMP543非常容易形成多晶型,通过粉末X射线衍射表征了17种多晶型。作者将DMP543形成如此多晶型的能力归因于其吡啶基团的构象灵活性,尽管后期确定分子灵活性与多晶型倾向之间没有统计相关性。研究发现,一些多晶型在加热时容易相互转换。但更有趣的是,显然相同的重结晶条件并不总是导致形成相同的多晶型。最终使用乙酸乙酯/庚烷混合溶剂建立了一种单一晶型的稳健结晶方法。然而,第一批次生产出了一种以前未得到过的晶型(#18)。尽管该方法最初看起来是稳定可靠的,但研究人员担心混合溶剂导致无法稳定制备晶型,并且在后续的实验中,不同的溶剂蒸发速率可能会触发其他新的、并不需要的晶型。因此科学家们决定基于单一溶剂对结晶工艺开发。随后发现,异丙醇能够可靠地高产率生产另一种新的多晶型(#19,Form A),该晶型最终被选择用于进一步开发。
在第一批Form A制备完成后,DMP543的合成工艺得到了改进,并利用这一改进的工艺制备了第二批。第二批的合成开始于美国新泽西州,但后期转移至临床试验开展地魁北克完成。在合成过程中,蒽酮烷基化剂必须经过三次纯化(通过两次重结晶和一次色谱纯化),然后从异丙醇中重结晶,以达到98.5%的纯度,这是临床试验可接受的最低纯度规格。然而,固体的第二次重结晶后出现了新的多晶型(#20,Form B)。随后使用Form A的晶种进行了三次重结晶,希望生产大批量的Form A,但所有实验都得到了Form B。当杜邦公司尝试再次制备Form A时,结果也完全形成了Form B。后来,杜邦公司再也无法生产Form A。根据热分析,Form B被证明是所有多晶型中最稳定的,因此被选为DMP543生产的优选晶型。尽管在接下来的五年中没有发现更多新的多晶型,但DMP543从未商业化过。
3.7 LAB687
另一个关于多晶型不可预测性的案例来自诺华,内部化合物涉代号为LAB687(图6a),这是一种用于控制甘油三酯和低密度脂蛋白胆固醇水平的微粒体甘油三酯转移蛋白抑制剂。在药物开发过程中发现了两种多晶型:原始合成路线产生了Form B,而基于不同工艺的克级合成得到了Form A。
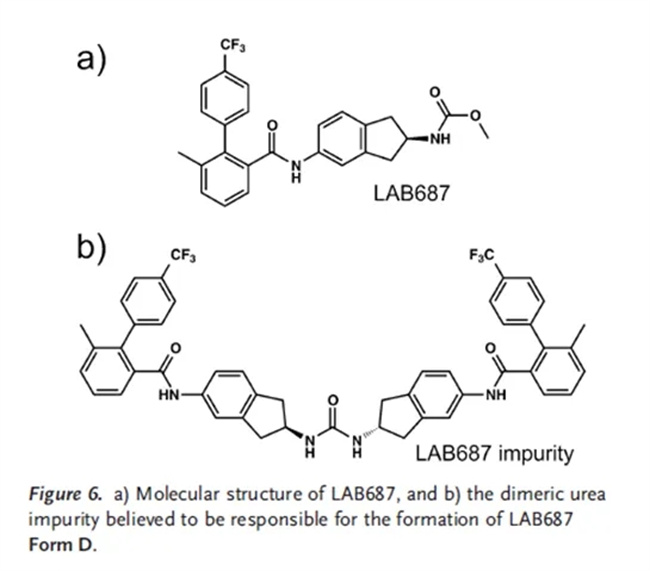
随后使用纯度为98.9%的Form A为起始进行了多晶型筛选,结果产生了第三种晶型(Form C)以及一种甲苯溶剂化物。在基于晶种加入的情况下,对Form A和Form C进行重复制备(100克规模)中,又发现了两种庚烷甲基环己烷的溶剂化物。Form A和Form C具有相似的溶解度和物理稳定性,但晶型C的粉体学性质更优于晶型A,因此选择Form C进行进一步开发。值得注意的是,一旦出现了Form A和Form C,Form B就无法再制备出来。但当Form C的结晶工艺被放大用于多公斤合成时,意外地出现了一种新的多晶型Form D。奇怪的是,一旦Form D出现,Form A和Form C就无法再制备。据推测,Form D的出现是由于在实施一种新的、更高效的合成路线时,LAB687批次的杂质谱发生了变化。实际上,这种路线导致了一种二聚尿素副产物(即杂质,图6b)的形成,这种杂质在使用其他合成路线获得的批次中不存在,尽管无法确定这种杂质的形成与Form D的出现之间的直接相关性。
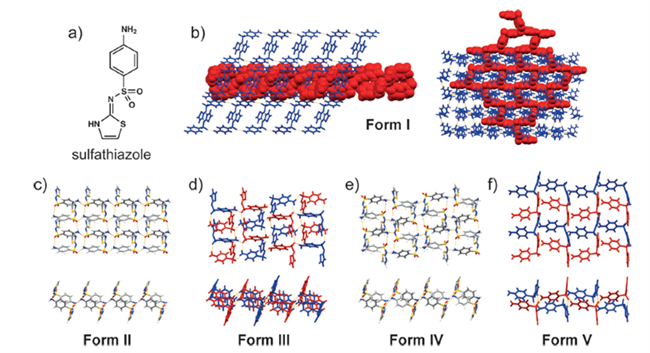
3.8 磺胺噻唑
抗菌化合物磺胺噻唑(图7a)多晶型现象也是由杂质或反应副产物引发的。迄今为止,已经鉴定出五种磺胺噻唑多晶型(图7b–f),以及超过一百种溶剂化物。磺胺噻唑各多晶型的固态性质已被彻底分析,并且许多研究小组都报告了制备每种晶型的不同方法。然而,也有报道称,某些方法不能可靠地用于制备目标磺胺噻唑多晶型的相纯批次,因为不同的研究小组使用相同的结晶条件报告了不同的结果。
有研究员分享了他从2000多次磺胺噻唑结晶实验中获得晶型结果的经验,并指出几乎使用的所有溶剂都可以获得所有五种已知多晶型。还指出,这些多晶型是互变关系,并且结晶后对固体的后处理直接决定多晶型结果。事实上,磺胺噻唑固体对结晶后处理的敏感性与文献中报告的不一致结果一致,这表明相同(或非常相似)的结晶条件可能导致不同磺胺噻唑多晶型的形成。
尽管报道中的结晶结果存在不一致性,但已经确定磺胺噻唑从水中结晶遵循Ostwald's规则,其中最不稳定的晶型(Form I)首先出现,然后转化为Form II和Form III,最终转化为热力学稳定的Form IV。尽管磺胺噻唑多晶型不像本综述中描述的其他多晶型那样“永久消失”,但磺胺噻唑系统因其复杂性和敏感性而显得独特,并强调了理解目标化合物合成过程中获得的副产物如何深刻影响其固态化学的重要性。
04 展望
从本综述的内容中应该可以明显看出,多晶型和多晶型转变几乎无法预测,并且不受控制的多晶型转化,可能对潜在API开发产生严重影响。有时很难理解为什么在晶型筛选完成后很长时间后,仍然会出现新的多晶型(而之前稳定的晶型消失)。关键在于,永远无法确定地说已经找到了最稳定的晶体形式;最多只能确定已知形式中哪一种是最稳定的。正如本文说的,一种新的(通常更稳定的)形式可以在化合物历史(或药物生命周期)的任何阶段出现。
没有标准的策略或万无一失的方案来寻找最稳定的晶型。精心设计的手动结晶实验与自动化高通量筛选相结合,可以减少但无法完全消除意外多晶型转变的可能性。在合成目标化合物时获得的所有易于获取的“重要”副产物都应考虑用作晶种。需要在压力条件下(例如极端湿度、温度和压力)筛选可能的多晶型转变,以增强产品在离开受控实验室空间后的稳定性信心。此外,应在药物或特种化学品的整个生命周期中考虑筛选和固态研究,以允许可能需要大量时间成核的新晶型的出现。
尽管与晶型筛选、分析仪器和计算机模拟方法相关的技术进步已经取得了显著的进展,但我们常常被迫回到对晶体成核和生长知识的基础问题上。20年后,我们中的一些人(或许多人)是否仍然会被多晶型和结晶的不可预测性“吓到”——或者到那时一切都会解决?仍然有许多挑战和惊喜在等待着我们。