


2024年,FDA共批准50款新药 [1],包含34款新分子实体,其中28款为小分子新药。从给药途径和剂型来看,在这28款获批的小分子新药中,4款为液体制剂(其中包括3款注射剂,1款口服溶液),2款为混悬剂(其中包括1款吸入混悬剂,1款口服混悬剂),22款为固体/半固体制剂(其中包括20款固体制剂,2款凝胶剂),如下表1。
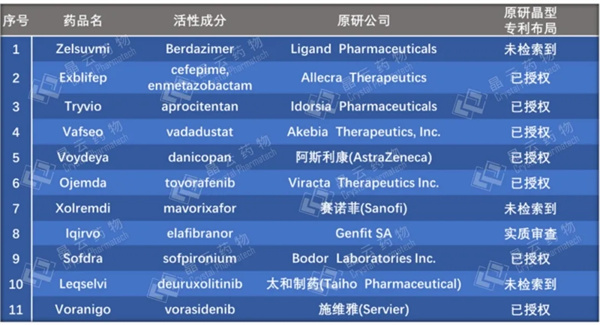
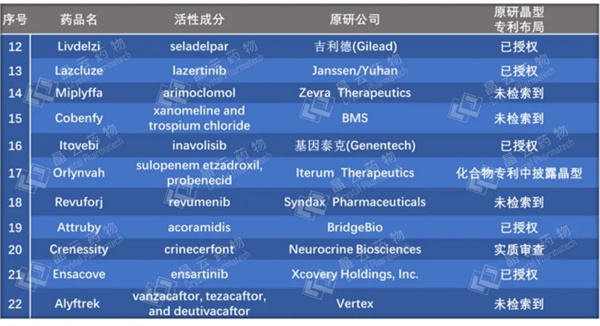
表1. 2024年FDA批准的34款新分子实体基本信息



通过对22款固体/半固体制剂小分子新药的原研公司专利布局分析发现,共有15款产品已经布局了晶型专利(统计包括正在审查中的专利),占所有固体制剂/半固体制剂小分子新药的68%,具体信息见表2。
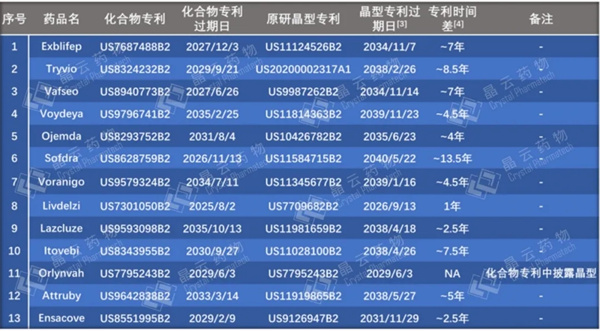
针对上述15款原研已有晶型专利布局的小分子新药,我们进一步分析了其化合物专利和晶型专利过期日及二者的时间差,结果见表3。未统计原研晶型专利还处于审查阶段的2个品种。有1个品种(Orlynvah)晶型相关信息已在化合物专利中被披露,另外12款品种原研晶型专利过期日均晚于化合物专利过期日,且晶型专利过期日和化合物专利过期日的时间差均大于1年,时间差在3年(含3年)以上的有9个品种,时间差在5年(含5年)以上的有6个。值得注意的是,Sofdra这个品种因晶型专利的布局而增加了长达13年的专利保护期。
表3. 13个小分子新药的化合物专利和晶型专利分析
小编从上述13个品种中选取2个品种作为代表,进行详细介绍,以帮助读者更好理解创新药公司如何通过晶型专利布局延长产品生命周期。这2个品种的获批也极具里程碑式的意义,无论是从治疗疾病本身还是市场份额预估,都是集极具潜力的重磅品种。
Voranigo
Voranigo (Vorasidenib)是由Servier研发的用于携带异柠檬酸脱氢酶(IDH)1或2突变的2级星形细胞瘤或少突神经胶质瘤的12岁及以上成人和儿童患者的手术(包括活检、次全切除术或全切除术)后治疗的处方药,也是FDA批准的首个且唯一一款用于治疗IDH突变2级胶质瘤的靶向药物。在IDH突变胶质瘤中,VORANIGO®通过抑制突变IDH1和IDH2酶的活性,帮助控制疾病进展。2024年8月6日,Servier宣布美国FDA已批准VORANIGO®上市,标志着胶质瘤治疗迎来重大突破。
上市产品中的药物活性成分为Vorasidenib的半柠檬酸半水合物共晶体,其化合物专利(US9579324B2)将于2034年7月11日过期,晶型专利(US11345677B2)披露了Vorasidenib与柠檬酸形成共晶的晶型,过期日为2039年1月16日。原研公司在该药物晶型专利上的布局使得该药物在化合物专利过期后仍有约4.5年的专利保护期。
Sofdra
Sofdra (Sofpironium)是由Bodor Laboratories Inc.开发的用于治疗成人和9岁及以上儿童的原发性腋窝多汗症的外用凝胶。这是FDA批准治疗这一症状的首款新分子实体。数据显示,多汗症是继痤疮和特应性皮炎之后的第三大皮肤病。现有治疗方法包括局部治疗,如使用含有抑汗成分的特定护理产品,或者系统性治疗,如口服药物或注射肌肉松弛剂。对于严重病例,还可以考虑手术治疗。抗胆碱能药物Sofdra的局部使用有助于减少系统性药物带来的副作用风险,并且在多项临床研究中已显示出显著的抑汗效果和良好的耐受性。在Sofdra获批之前,FDA 批准用于多汗症的唯一外用抗胆碱能药物是 2018 年批准的甲苯磺酸甘珀罗铵(Qbrexza)。2024年6月18日,Botanix公司宣布美国FDA已批准Sofdra上市。
上市产品中的药物活性成分为结晶形式的Sofpironium。其化合物专利(US8628759B2)将于2026年11月13日到期。晶型专利(US11584715B2)披露了化合物Sofpironium的Form A、Form MN、Form MJ、Form CO、Form B各多晶型,过期日为2040年5月22日。原研公司在该药物晶型专利上的布局使得该药物在化合物专利过期后仍有长达13.5年的专利保护期。
总结
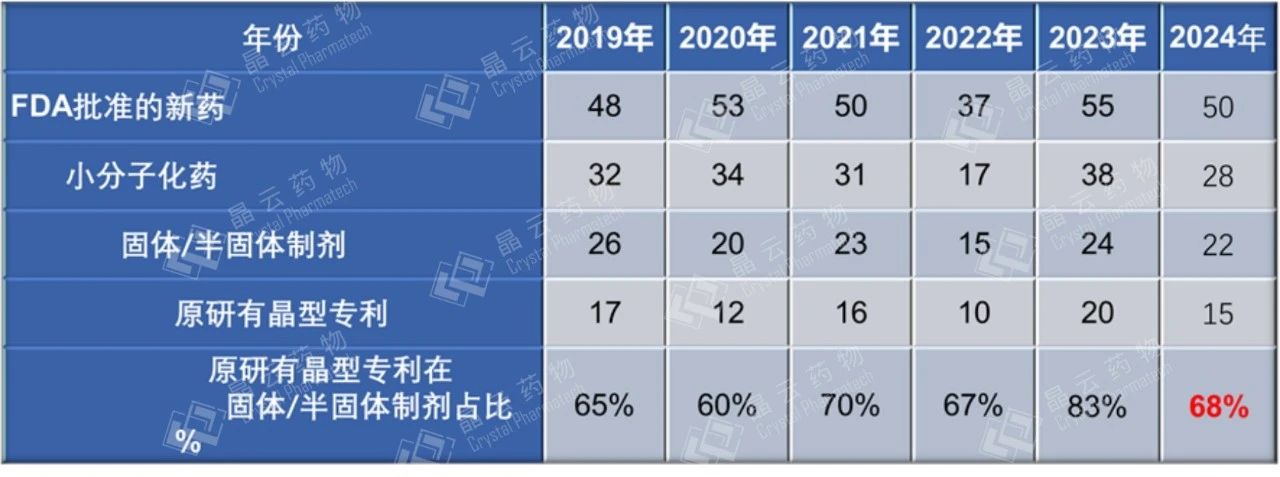
回顾近6年的数据(表4),虽然小分子化药获批的个数略低于去年,但固体/半固体制剂的小分子新药仍然保持在与前五年相近的水平。同时也可以观察到,近几年原研有晶型专利布局的产品比例稳定维持在60%-80%的区间,不难看出创新药公司在新药开发过程中对于药物晶型的研究和晶型专利布局的重视。其一是因为药物晶型直接对药物的生物利用度、稳定性以及工艺可开发性带来的影响,对于晶型的质量控制越来越多地成为是监管部门在小分子新药申报时关注的重点。其二,对创新药企业来说,扎实的晶型专利有助于建立更高的技术壁垒来抵御仿制药企业的竞争,延长新药的专利保护期,从而获取更长期的市场经济效益。
表4.近6年FDA批准新药的晶型专利保护情况
参考文献及标注
[1] https://www.fda.gov/drugs/novel-drug-approvals-fda/novel-drug-approvals-2024
[2] 化合物专利过期日以橙皮书记载的过期日为准:https://www.accessdata.fda.gov/scripts/cder/ob/index.cfm.
[3] 对于已授权专利,以官方公布的过期日为准。
[4] 晶型专利过期日减化合物专利过期日。