

前情回顾
上篇就外消旋化合物和外消旋混合物三元相图进行了初步解读,那对于实际拆分中如何运用三相图的原理帮助理解工艺过程,调节控制参数实现最大拆分效率,在今天的应用以及实际案例中将为各位读者作进一步解读。
内容导览
8. 三元相图在优先结晶中的应用
8.1 一步结晶法
8.2 连续优先结晶
8.3 外消旋化合物优先结晶
8.4 优先结晶影响因素
9. 三元相图在化学拆分中的应用
9.1 非对映体盐/共晶拆分思路
9.2 化学拆分影响因素
9.3 非对映体盐结晶拆分案例
10. 总结
8
三元相图在优先结晶法的应用
8.1 一步结晶法(仅需某一种构型的异构体)
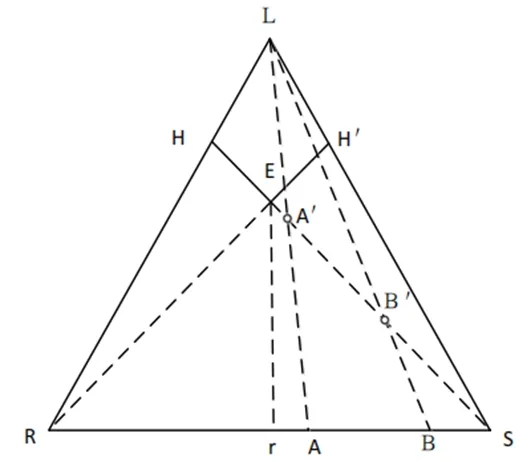
图1. 一步优先结晶法拆分外消旋混合物
如图1所示,若初始外消旋体系的光学组成为A,起始ee值为ee0,向体系中加入溶剂,溶液组成沿AL向L点移动,体系组成由区域SRE向ESH’过渡,A’点恰为临界点,此时仅S构型结晶析出,R构型溶解在液相中,对应所加溶剂体系为Vmin,此浓度下结晶所得S构型的产率最高,对应公式为:
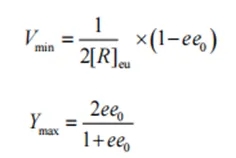
因此,初始外消旋混合物的光学纯度越高(从A点到B点),则Vmin越小,溶液浓度越高,相应的得到的S构型产率越高,溶液结晶的可操作性区域更大,更有利于拆分的进行。
8.2 连续优先结晶(两种构型的异构体均可结晶)
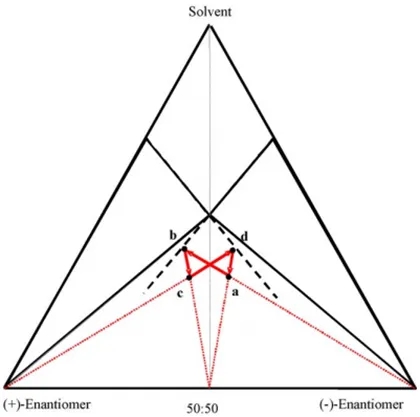
图2. 连续优先结晶拆分外消旋混合物
如图2所示,初始外消旋体系中的光学组成为a,(-)对映体过量,起始ee值为ee0,在加入(-)对映体后,其对应的过饱和度将提升,体系成分组成变化轨迹将由a到b,一旦超过b点,另一种构型将会自发结晶析出,形成混合物。因此,在这个过程发生之前就需把(-)对映体及时分离出。同时,向溶液中补加等量的外消旋化合物,溶液组成将由轨迹从b到c,同理,向体系中加(+)对映体,体系成分组成变化轨迹将由c到d,(+)对映体结晶析出。此区域内重复上述操作即可得到两种纯对映体产品。
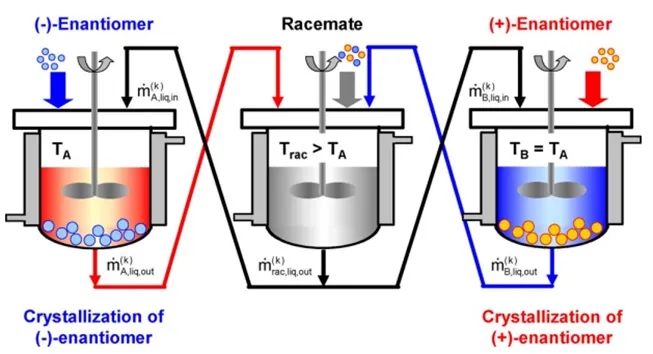
图3. 连续优先结晶拆分在工业中应用
8.3 外消旋化合物的优先结晶
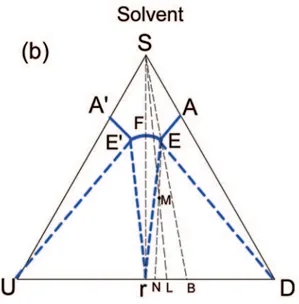
图4. 外消旋化合物的优先结晶拆分
根据上述部分对外消旋混合物的解读,进一步分析外消旋化合物是否也适合用优先结晶的方法实现ee值提升。理论上是可行的,但存在相应限制条件,即起始外消旋体系的ee值需高于共晶点E的ee值。如图4所示,若起始固体组成落在B-D之间,通过加溶剂调节总组分还可以从EBD区域跨度到AED的优先结晶区域,这种情况下类似聚集体的拆分操作,所加溶剂体系体积和对应理想构型产物的产率遵循以下公式:
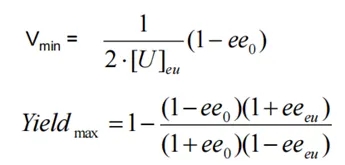
但若起始固体组成落在r-B之间,那在调节总组分过程中会经过固相到只含外消旋化合物的两相区ErF,此时D将全部溶解,固相只剩外消旋化合物,上清液的ee值将低于共晶点ee值。所以整个操作下来体系所能达到的ee值最大为共晶点E的ee值,所加溶剂体系体积和对应理想构型产物的产率遵循以下公式。若远不能达到理想的ee值提升,这种情况下就需要考虑其他的方法来实现拆分(非对映体盐结晶拆分的思路)。
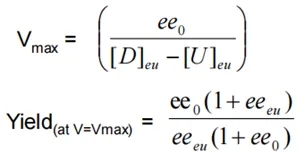
8.4 优先结晶的影响因素
a) 外消旋混合物本身性质:外消旋体的盐(如盐酸盐、硫酸盐等)比形成共价外消旋体更容易通过优先结晶拆分;初始体系本身的光学纯度也会影响拆分产率;溶解度比(外消旋体的溶解度与一种对映异构体的溶解度比值)比值小于2时比大于2更有利于优先结晶,这是因为当外消旋体的溶解度小于纯异构体的溶解度时,可扩大溶解度曲线图中可用于优先结晶的区域;
b) 结晶过程的控制:该结晶过程类似溶液结晶,需要严格控制溶液体系的过饱和度释放和亚稳区间,通过调节参数,如搅拌速度,晶种添加时间/量,溶剂添加速率/量以及温度等,控制非需要的异构体能始终稳定存在于溶液中。
9
三元相图在非对映体盐/共晶拆分法的应用
9.1 非对映体盐/共晶拆分思路
对于成盐体系来说,外消旋化合物与手性拆分剂形成的是非对映异构体(如RR’和SR’),它们的理化性质存在差异,因而三元相图也是非对称的。通过对拆分剂的筛选,同时可构建不同体系下的三元相图,对比结晶可操作空间来选择最优的拆分试剂。如下图5所示,Sistla等人以DL-丝氨酸苄酯为拆分化合物,详细研究了几种拆分试剂的拆分效果。通过构建两个非对映体盐在溶剂体系中的三元溶解相图,发现起始化合物与2,3-二苯甲酰-L-酒石酸形成的体系中优先结晶区域最大(阴影区域),拆分可操作性最好,另外两种体系均不能实现比较好的拆分效果。当然在实际的拆分实验过程当中,往往会选择多个拆分体系,通过HPLC的方法来测定ee值,直观地获得拆分效果最好的体系。三元相图只是在这个过程当中,能够帮助我们去更好地从原理上去理解反应过程,并对后续的结晶控制的环节提供一些参考思路。
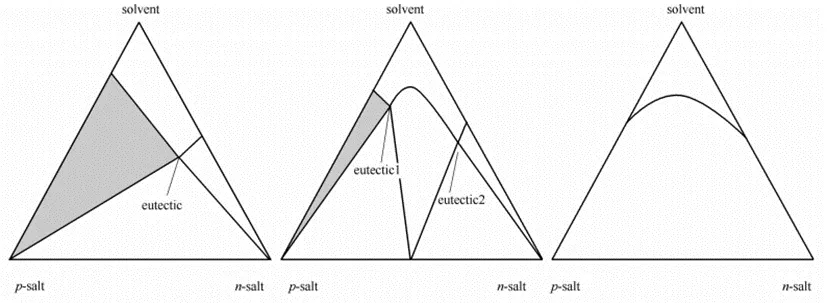
图5. 不同拆分体系下非对映体混合物的三元相图
当筛选到比较好的拆分剂后,接下来就是通过优化溶剂,加光学纯的非对映体盐的晶种等方式使整个结晶过程能停留在优先结晶的区域中,并且能够实现较大产率。这也就回到了我们之前讨论的优先结晶相关的影响因素,即涉及到对整个结晶过程中不饱和度释放以及亚稳区间的控制来实现光学纯的异构体最大收率。
9.2 化学拆分影响因素
除了考察结晶因素的影响外,是否还存在其他因素也影响着化学拆分的拆分效率呢?显而易见,从我们整个化学拆分的操作步骤来看还存在着其他变量,例如手性拆分试剂的选择,拆分剂与底物的当量比,溶剂体系等。
拆分试剂选择:一般来说,拆分试剂的选择需要具备三个原则——1) 光学纯度高,经济易得;2) 能与被拆分底物形成非对映体盐或共晶,且拆分后容易破盐去除;3) 形成的非对映体盐或共晶的溶解度差异显著。对于碱性化合物而言,一般按照上述原则选择酸性配体。其中,酒石酸及其衍生物是最常用的拆分试剂之一,一般认为引入多个极性基团,且与关键官能团临近,在形成非对映体盐时,可形成两个以上的接触点,提高拆分能力。SAKAI等人发现,以酒石酸作为拆分剂对外消旋底物进行拆分时,识别机制可能为酒石酸分子首尾相连,形成了一个特异性的手性识别区,在此区域内只允许其中一种构型容纳其中并形成晶体析出,从而实现拆分。而对于酒石酸衍生物,如二苯甲酰酒石酸、二对甲氧基苯甲酰酒石酸、对甲基二苯甲酰酒石酸等,因其在空间上引入了大位阻官能团,在长链基础上引入新的氢键、空间位阻以及疏水作用力使得手性识别区的识别能力增强,从而进一步提高手性拆分的效率。对于手性酸化合物拆分则通常选用手性生物碱、氨基酸及其衍生物。
拆分溶剂体系选择:从小编个人角度来看,拆分溶剂体系的选择略显微妙但却是整个拆分过程中尤为重要的一环,需要建立在操作人员对于化合物溶解度足够了解、项目经验足够丰富的基础上,才能从广泛的溶剂体系中敏锐地找到合适的体系(可以是单一溶剂体系、也可以是混合溶剂体系)来合理设置拆分方案,并通过后续的实验摸索找到优选的拆分体系。这里的微妙之处也就在于首先选择出的溶剂需要具有一定的溶解能力去溶解外消旋体,从而与手性配体成盐,同时这个溶剂体系需要恰好满足理想型的非对映异构体能够结晶析出,而另一种构型的盐则能很好的溶解其中,实现最大拆分效率(理想构型产物具有高手性纯度,和接近50%的理想产率)。随着手性拆分研究的发展,也有研究者提出一些理论概念作为参考支持,除了为大家所广泛接受的分子立体化学理论,SAKAI等人于2007年提出了“由溶剂介电常数控制的拆分”(DCR)理论,从分子层面对拆分机理做出系统的解释,如下图6所示。在非对映体结晶的过程中,手性拆分试剂分别在两种构型的非对映体盐的分子组装很相似,即拆分试剂的亲水基团(极性基团)会聚集形成具有选择性的手性识别区间(即下图(a)和(b)中II的空腔),但因其空隙不同(与不同基团间的作用力相关,如氢键、分子间作用力等)从而会对不同构型的非对映体盐起到选择性识别的作用,每个优先识别的构型分子将会填充在每个空腔中,紧密堆积并结晶析出,而另一种未被识别的构型则游离在溶液中,从而实现拆分。正因如此,所选溶剂的介电常数将会通过影响分子作用力进而影响手性识别区间大小,研究者通过考察不同介电常数的溶剂对拆分结果的影响,结合晶体学数据支持,得出一个普适性的结论——溶剂介电常数大小与手性识别区间中的空隙成正比。因此,可以通过调节溶剂体系的介电常数,使得空腔的分子识别更为“精准”(对应手性纯度提升),甚至可能实现“拆分逆转”,得到相反构型的非对映体盐的析出晶体。
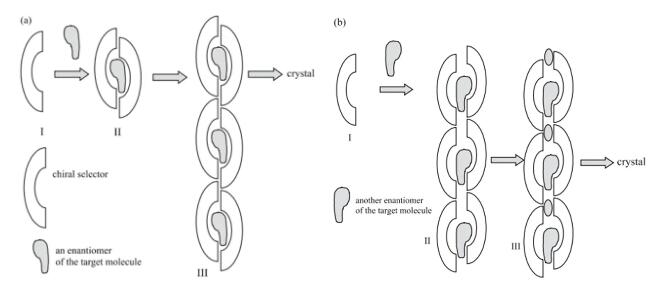
图6. DCR的分子机制
图6. DCR的分子机制:(a)介电常数小的溶剂中形成的手性识别区间较小,特异性识别一种构型分子填充其中,紧密堆积后结晶析出;(b) 介电常数大的溶剂中手性拆分剂分子的亲水基团间距增大,产生不同的手性环境,使得原本可以识别的构型无法再被识别,另一种构型的分子正好因此而被识别。这种情况下的手性拆分剂分子之间的堆积不够紧密,不足以形成一个实质性的空腔,如果存在水等小分子来填补这个空隙,实现紧密堆积,就能使另一种构型的非对映体盐结晶析出。
拆分试剂与底物当量比:根据拆分剂与底物的不同比例,化学拆分法可以分为半量拆分(拆分试剂与底物当量比为0.5)、全量拆分(拆分试剂与底物等量)和过量拆分(拆分试剂过量),理论上来说1当量外消旋体拆分只需要0.5当量的拆分试剂,但实际情况中需要考虑到溶剂、拆分剂分子与底物分子的相互作用,所以需要用试验摸索考察合适的当量比。FERREIRA等人发现,运用二元手性酸拆分一元碱时,需要特别注意二元酸的用量。由于其存在两个羧基,当酸与底物的当量比小于1:2时,体系趋于形成中性盐(1分子羧酸的两个羧基均与底物结合成盐);而当酸与底物的当量比大于1:1.5时,体系趋于形成酸式盐。两种类型的盐在同一溶剂体系中的溶解度存在差异,也就导致拆分结果存在差异;同时,在形成中性盐时,羧基结合两个碱基是不存在手性识别机制的,而是随机结合,这样也就导致形成的中性盐可能结合了两个不同构型的底物,从而大大影响了最终产品的手性纯度。所以考察拆分条件时,当量比是一个很关键的考察项,不容忽视,特别是在使用了二元手性酸的情况下。
9.3 非对映体盐结晶拆分案例分享
综合考虑拆分体系筛选和结晶的两个过程,完整的手性拆分工艺流程也就此显现。在此,小编也再通过实际的一个案例分享来进一步解析整个工艺流程。该项目是开发化合物X手性拆分工艺。
拆分体系初步筛选:根据化合物性质(如pKa,溶解度等)选择25个手性配体,4个溶剂体系共100个成盐筛选试验,通过测试计算上清液中杂质构型与目标构型的峰面积比,初步筛选具有拆分效果的拆分体系。发现化合物在配体C/溶剂A,配体E/溶剂C和配体F/溶剂B三个体系中具有比较好的拆分效率,但在与配体F成盐实验中,在多个溶剂条件下观察到成胶的现象,不利于后续工艺开发,配体C成盐实验中,上清液中理想构型比例更高。因此,初步筛选得到优选的配体E/溶剂C拆分体系。
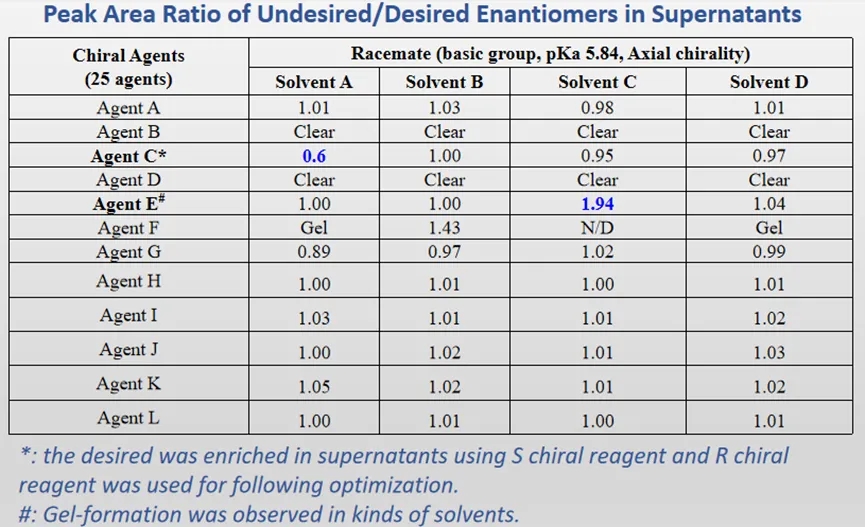
图7. 拆分体系初步筛选
拆分体系进一步筛选(多个拆分因素考察):在这一轮筛选方案设置中,进一步考察了溶剂体系、当量比对拆分效率的影响。以确定的配体E,首先考察了在单一溶剂情况下杂质构型与目标构型的比例,结果发现在溶剂C的条件下,杂质构型与目标构型的溶解度存在最大差异,但两种构型的在该溶剂体系下的溶解度都很小,无法开展后续的溶液结晶,所以需要进一步优化。因此,再一次考察混合溶剂是否能够解决当下问题,通过几种二元溶剂体系的筛选得到了溶剂C/B的混合体系,在保证溶解度满足需求的情况下且两种构型含量存在最大差异,可以进行后续的拆分工艺研究。
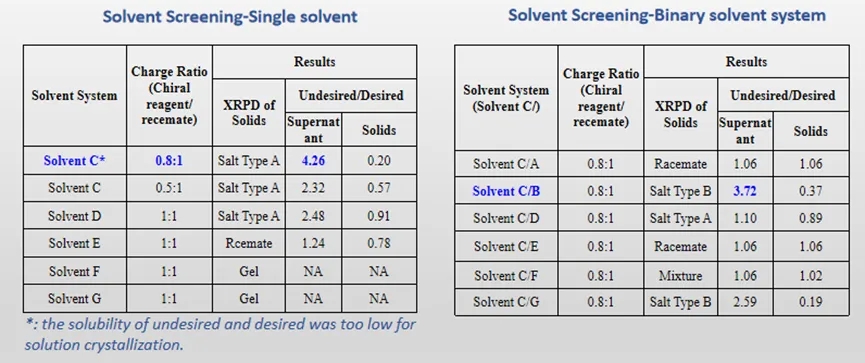
图8. 拆分体系进一步筛选(多个拆分因素考察)
拆分体系优化:那所选择的混合溶剂的组分比例是否为最佳呢?那还需要进一步考察验证不同比例的溶剂C/B体系的拆分效率。通过对比在50%,66.7%,80%,90%四个比例的溶剂C/B中上清液杂质构型与目标构型的溶解度比,发现在比例为66.7%的体系中对应的比例最大,最终平衡状态下目标构型的理论产率最高;通过对比固体的ee值,同样也发现在比例为66.7%的体系中对应固体产品的ee值最高,且达到平衡的时间相对较短。因此,经过这一步的优化,确认该组分比例的混合溶剂体系为拆分工艺的优选溶剂体系。
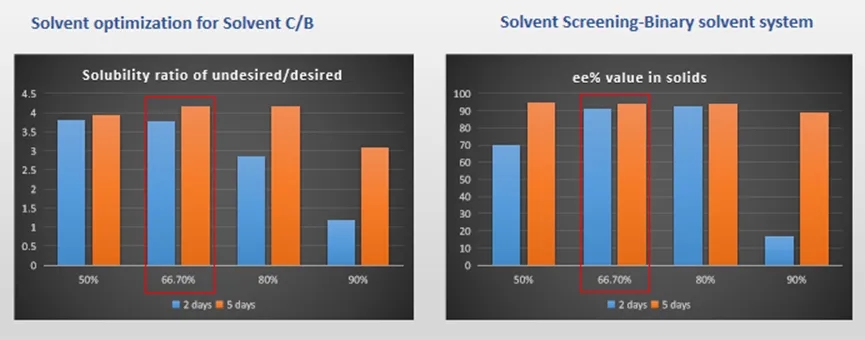
图9. 混合溶剂组分比例对拆分效率的影响(溶解度比/ee值)
手性拆分工艺验证:根据筛选和优化的结果,确定了最佳拆分体系。对此进一步展开结晶工艺验证,尝试了0.5 g和1 g两个克级规模的溶液结晶工艺研究,尝试5 ℃和20 ℃两个终点结晶温度,最终在降温至20 ℃体系中获得的固体产品具有99.0%的ee值和66%的实际产率,实现项目目标。
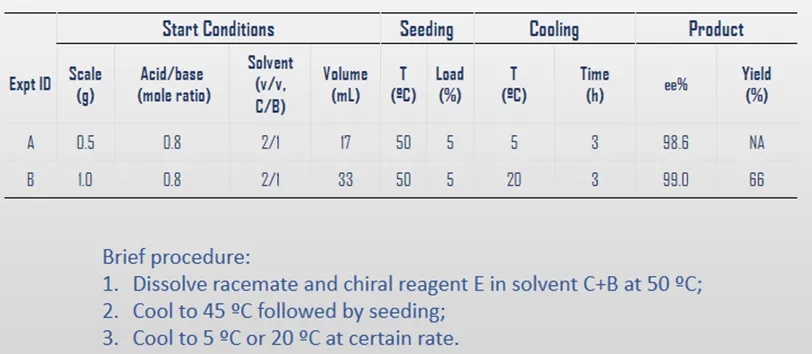
图10. 手性拆分工艺验证
在实际开展手性拆分工艺研究时,往往会因化合物本身性质而使每个项目都会具有一定的特殊性,实际的方案设置也会存在较大差异,所以需要我们的实验人员对于三元相图、结晶工艺等原理有较好的理解,同时也需要建立在有丰富的拆分项目经验上才会有清晰的解决思路,开发出一个合适的手性拆分工艺。
10
结语
总的来说,手性药物拆分不论从药物本身层面还是监管层面都将是一个趋势,它也将对制药工业中现行的手性拆分方法提出更高的要求。不同的拆分方法都有相应的局限性,也需要在后续不断的研究摸索中实现优化。
那对于现有的拆分方法,怎么样去选择适合手性化合物的最佳方法呢?小编这边也按照个人理解,整理相关的workflow,也希望和业界同行一起讨论交流。
1. 外消旋体类型的判断-可以通过前文介绍的图谱法对比(如红外、XRPD、DSC、单晶等表征),二元熔点相图、三元溶解度相图等方法。一般来说,外消旋混合物和外消旋化合物基本可以通过图谱法进行准确判断。
2. 对于外消旋混合物,可以考虑用优先结晶的方法,通过调节结晶工艺参数实现比较高产率回收单一异构体;
3. 对于外消旋化合物,可以先判断起始外消旋体的ee值。若其大于共晶点ee值,可以考虑优先结晶的方法;若共晶点ee值>需求ee值>起始ee值,也可以考虑用优先结晶;若起始ee值<共晶ee值<需求ee值,则需要用非对映盐/共晶结晶的方法实现拆分。
晶云药物研发团队在手性拆分项目研究中已积累了多年实践经验,同时我们也期待在手性拆分领域中与业界同行有更多的交流探讨。
参考文献
[1]. 尤启冬,林国强. 手性药物研究与评价[M]. 北京:化学工业出版社,2011: 143-144.
[2]. SAKAI K, SAKURAI R, HIRAYAMA N. Molecular mechanisums of dielectrically controlled resolution [J]. Topics in Current Chemistry, 2007, 7 (269): 233-271.
[3]. SAKURAI R, YUZAWA A, SAKAI A. Dielectricallycontrolled enantiomeric resolution of (R) -and(S) -2-methylpyrrolidine by (R, R) -tartaric acid [J]. Crystal Growth & Design, 2006, 6(7): 1606-1610.
[4]. FERREIRA F C, CHAZALI N F, COCCHINI U, et al. Rational approach to the selection of conditions for diastereomeric resolution of chiral amines by diacid resolving agents [J]. Tetrahedron Asymmetry, 2006, 17(9): 1337-1348.
[5]. Sakai K, Yokoyama M, Sakurai R,et al. Resolution of 1-cyclohexylethylamine via diastereomeric salt formation with enantiopure 2-phenylacetic acids[J]. Tetrahedron Asymmetry, 2006, 17(10): 1541–1543.
[6]. Ferreira F C, Ghazali N F, Cocchini U,et al. Rational approach to the selection of conditions for diastereomeric resolution of chiral amines by diacid resolving agents[J]. Tetrahedron: Asymmetry, 2006, 17( 9): 1337-1348.
[7]. 邓艳芳,吴桐,李泽文,等.手性拆分技术-化学拆分法的研究进展[J].沈阳药科大学学报, 2019(11):5.