

随着药物机理复杂性的提高,对生物利用度和PK提出了更多的挑战,仅仅依靠速释制剂已经无法满足药效的要求。缓控释制剂因具有用药次数少、降低药物毒副作用等优点,成为近30多年来研究的热点,并获得了广泛的应用。本文将从缓控释制剂的基本概念、常见的分类、以及影响口服缓控释制剂设计的常见因素几个方面,为大家介绍。
基本概念
根据《中国药典》2020年版中的定义,调释制剂系指与普通制剂相比,通过技术手段调节药物的释放速率、释放部位或释放时间的一大类制剂。调释制剂可分为缓释、控释和迟释制剂等。其中,缓释、控释制剂与普通制剂比较,药物治疗作用更持久、毒副作用可能降低、用药次数减少,可提高患者用药依从性。迟释制剂可延迟释放药物,从而发挥肠溶、结肠定位或脉冲释放等功能。
缓释制剂系指在规定的释放介质中,按要求缓慢地非恒速释放药物,与相应的普通制剂比较,给药频率减少一半或有所减少,且能显著增加患者用药依从性的制剂。
控释制剂系指在规定的释放介质中,按要求缓慢地恒速释放药物,与相应的普通制剂比较,给药频率减少一半或有所减少,血药浓度比缓释制剂更加平稳,且能显著增加患者用药依从性的制剂。
迟释制剂系指在给药后不立即释放药物的制剂,包括肠溶制剂、结肠定位和脉冲制剂等。广义上的控释制剂包括迟释制剂。
本文所指的缓控释制剂包括缓释、控释和迟释制剂。
缓控释制剂优点和不足
优点
1.延长给药间隔时间,减少服药频率,提高患者依从性。
2.维持平稳的血药浓度,减少对胃肠道的刺激,有利于降低药物的毒副作用。
3.增强疗效,减少用药总剂量,以最小剂量达到最大药效。
不足
1.适用范围:并非所有的药物都适合制成缓控释制剂。
2.剂量调整:在临床应用中对剂量调节的灵活性降低,如遇到特殊情况,不能立即停止治疗(一般不可掰服)。
3.给药方案调整:缓控释制剂是基于健康人群的平均动力学参数设计的,当药物在病理状态的体内动力学特征有所改变时,不能灵活调整给药方案。
4.口服缓控释制剂常常有食物效应,在食物影响下造成大的变异性。
5.生产方面:与普通速释制剂相比,成本较高,工艺技术复杂,价格较昂贵。
下图为药物的血药浓度-时间曲线的示例,某药物的治疗窗为C2-C1,若开发成普通制剂,其在t1-t2时间段的因超过了最低中毒浓度C1,存在较高毒副作用,并且在t3时,血药浓度已低于最低有效浓度C2,需要重新给药。若开发成缓释或控释制剂,因Cmax的降低,药物毒副作用减小,用药间隔也由t3延长到t4或者更长时间。
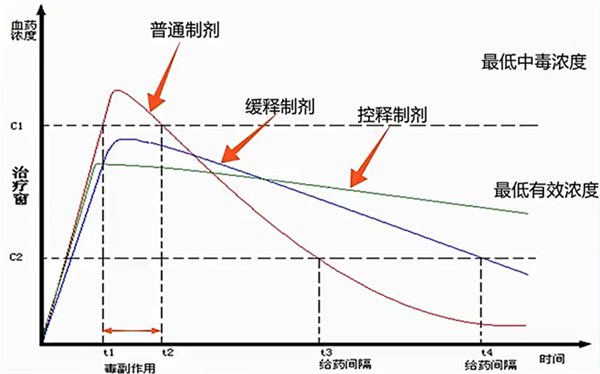
不同制剂技术的血药浓度-时间曲线
缓控释制剂的分类
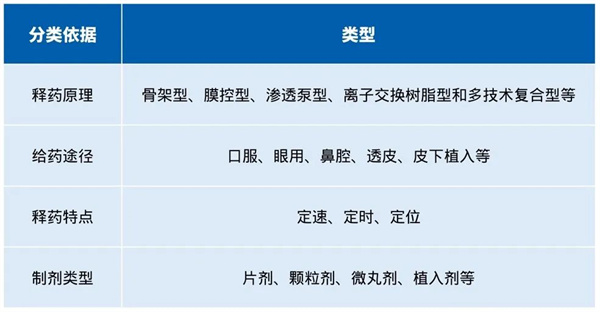
如下表所示,根据特定的分类依据,可将缓控释制剂细分为不同的类型。其中,按照释药原理进行的分类在实际应用中最为常见。下文将围绕释药原理的分类进行详细阐述。
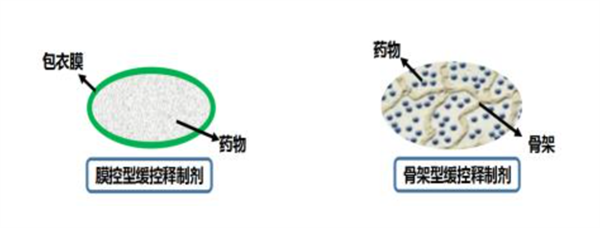
骨架型缓控释制剂是指药物(以晶体、无定形、分子分散体等形式)与控速材料及其他惰性成分均匀混合,通过特定工艺制成的固体制剂。制剂在水或生理体液中能维持或转变成整体式骨架结构,起到药物储库的作用,药物通过扩散或骨架溶蚀释放。骨架型缓释控释制剂因制备成本低且易于大生产,成为了口服缓控释制剂中应用最多的释药类型。
膜控型缓控释制剂通过包衣膜来控制制剂中药物的释放速度和释放行为。包衣对象通常为片剂、微丸。药物释放若是通过无孔膜的扩散,药物溶解度是影响药物释放的主要因素;若是通过有孔膜的扩散,调节致孔剂的用量可实现控制释药速率。
渗透泵型缓控释制剂是由药物、半透膜材料、渗透压活性物质和推动剂等组成的,以渗透压作为释药动力的制剂。
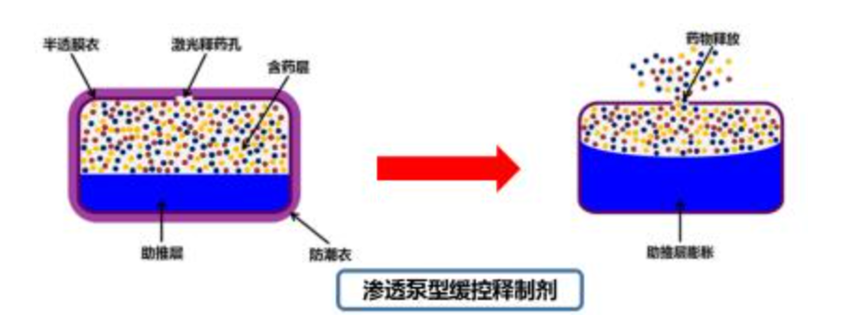
图片来源于参考资料3
影响口服缓控释制剂设计的因素
1. 药物理化性质
药物的理化性质,例如溶解度、解离常数pKa、分配系数logP和化学稳定性显著影响制剂的设计。由于药物优先以非解离形式转运穿过生物脂质膜,因此药物性质如pKa、logP、溶解度和胃肠道的生理环境之间的关系,对缓控释制剂的设计具有重要的意义。
溶解度
药物的溶解度限制了释放机理的选择,是设计缓控释制剂的最重要因素之一。溶解度太低的药物要考虑采用相应的增溶措施来增加溶出度和生物利用度,如微粉化、制备固体分散体和包合物等。具体参见解锁难溶性口服药物增溶方法。
解离常数pKa
药物的pKa反映了药物在不同pH环境下的解离程度。一般说来,非解离型的、脂溶性大的药物易通过脂性生物膜,胃肠道pH值和药物的pKa会影响药物的解离程度。
分配系数logP
logP高的药物,脂溶性好,水溶性差,易于进入生物膜。logP低的药物,则透过脂质膜较困难。因此,分配系数需要选择适中的,过大过小均不利于药物的吸收。口服药物通过被动扩散渗透时,logP 0-3范围最佳。
稳定性
口服药物同时受酸碱水解和酶降解作用的影响。在胃中不稳定的药物,可延缓释药时间,制成肠内释药制剂。在肠道中不稳定的药物,可以做成在胃中缓慢释放的制剂。即了解药物稳定性后,可通过制剂手段,合理控制释放区域。
2. 药动学及生物药剂学性质
药物在胃肠道不同部位的吸收特性以及制剂在肠道的滞留时间是影响口服吸收的重要因素。胃肠道不同部位的pH、表面积、膜通透性、分泌物、酶、水量等不同,在药物吸收过程中所起的作用可能有显著差异,因此在研发前需充分了解药物的生物半衰期、药物在胃肠道的吸收部位或吸收窗,并在处方设计时考虑如何减小可能的个体差异。
生物半衰期(t1/2)
t1/2是定量描述药物体内消除速率的重要生物药剂学参数,并且是缓控释制剂设计中考虑的标准之一。为了将治疗药物的血药浓度长时间维持在某一水平,药物吸收速率要与药物消除速率相差不大,这与药物的半衰期有关。通常,半衰期非常短、分布容积非常高的药物在体内会被迅速清除,使得延长释放时间和行为变得困难。一般来说,t1/2>12h,本身药效已较持久,一般不采用缓释制剂。t1/2过小,如t1/2<1h,不易(难度大)制成缓控释制剂。通常,t1/2在2~8h适合制成缓控释制剂。
吸收速度
制备缓控释制剂的目的是控制制剂的释药速度。大多数药物及其制剂在胃肠道的运行时间为8~12h,吸收半衰期近似于3~4h,如果药物释放过慢,药物还未全部释放时,制剂已离开吸收部位,造成制剂生物利用度降低。因此本身吸收速度常数很低的药物,不太适宜制备成缓控释制剂。
吸收部位
确定药物在胃肠道的部位非常重要,通常全肠道吸收的药物较适合制成缓控释制剂。如有些药物只在结肠或者胃部易吸收,可以通过制剂手段,使得药物运到相应部位后再释放。
代谢
在吸收前有代谢作用的药物,制成缓控释制剂生物利用度一般都会降低。因为大多数肠壁酶系统的药物代谢作用具有饱和性,如少量药物持续缓慢地释放到这些部位,酶的作用将使较多量的药物转变成代谢物,使得药物生物利用度明显降低。吸收前有代谢的药物,不适宜制成缓释制剂,如要制成缓释制剂,一般需加入代谢的抑制剂。
总结与展望
缓控释制剂作为一种特殊的释药系统一直受到广泛关注,适用于治疗窗窄、生物半衰期短、刺激性较大的药物,或者对药物依从性要求较高的需要长期用药的慢性病药物,如降压药,抗心率失常药,抗心绞痛药,抗哮喘药、抗精神失常药等。设计缓控释制剂时应考虑药物的理化性质、药动学及生物药剂学等性质,并结合临床需求进行可行性评价。
晶云药物CDMO事业部(晶云星空)具有丰富的缓控释制剂开发经验,拥有缓控释制剂技术平台,可提供包括骨架型、膜控型等缓控制剂开发和生产服务。可根据药物分子的理化性质、药学性质、临床需求及开发目标,为客户量身制定首次正确的缓控释制剂,剂型包括单层片、双层片、胶囊、微片等。晶云星空已成功为多个客户提供了缓控释制剂研发和生产服务,如利用微片缓控释技术在大鼠得到PK数据,帮助客户在临床前决策了首次人体试验(FIH)的剂型;利用双层片+肠溶包衣技术成功实现零级释放,实现了与渗透泵技术的片剂生物等效。如您有任何缓控释制剂开发需求,欢迎垂询。
CDMO事业部 - 专注制剂研发与生产服务
18015418250(王女士)
18015585433(刘女士)
18015584933(韩先生)
cfs@crystalpharmatech.com
参考资料
[1]《中国药典》2020年版
[2]书籍:《难溶性药物制剂技术》
[3]健康时报网:精神科药物到底能不能掰,看这些小窍门
[4]https://open.163.com/newview/movie/free?pid=THINITHVH&mid=KHIP982NF
原文请点击查阅