

随着小分子药物研究的不断深入,药物分子的结构设计越来越复杂,药物溶解性差成为了新药开发面临的重要问题。据文献报道1,目前上市的小分子药物中约40%为难溶性化合物,而研发阶段的药物,难溶性候选化合物占比接近90%。因此,改善药物溶解性、提高生物利用度成为新药研发亟待解决的难题之一。本文,小编将向大家介绍几种常用的难溶性口服药物增溶方法。
目前常用的方法有:成盐,多晶型,减小API粒径,制备无定形固体分散体,添加环糊精或表面活性剂等。
在详细介绍各种技术之前,我们需先了解一个重要的概念——药物可开发性分类系统(Developability Classification System,DCS),该系统可以指导研发人员确定药物分子是否需要增溶以及选择何种增溶方法。
01
什么是DCS
药物可开发性分类系统,与生物药剂学分类系统(Biopharmaceutics Classification System,BCS)分类类似,DCS也是根据溶解度和渗透性将药物分为4类。相比BCS系统,DCS对溶解性和渗透性的评价指标进行了优化,并对Ⅱ类进行了进一步划分。根据限制体内吸收因素不同,DCSⅡ类又分为DCSⅡa(溶出限制体内吸收)和DCSⅡb(溶解度限制体内吸收)。
对于DCSⅠ和Ⅲ类的药物,无需增溶,可以使用常规的制剂手段。而对于判定为DCSⅡa的化合物,一般可通过降低粒径等策略解决因溶出而造成的吸收障碍。对于判定为DCSⅡb和DCSⅣ类化合物,就需要采用其他的方法,例如成盐、制备亚稳多晶型或无定形固体分散体等,来提高药物溶解度和生物利用度。
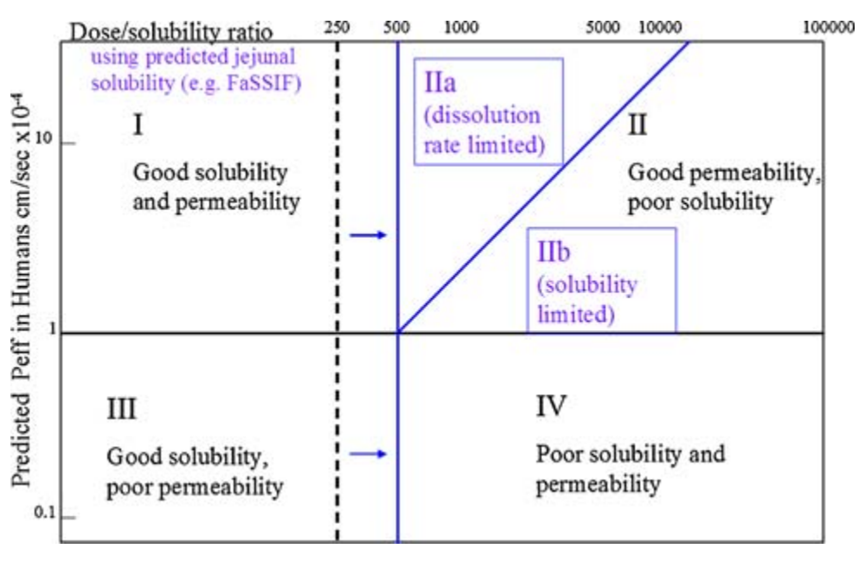
图片来源于参考文献3
02
常见的难溶口服药物
增溶方式
1. 成盐
药物成盐是一种简单且有成本效益的增溶方法,有机弱酸弱碱药物制成可溶性盐可增加溶解度,从而提高可电离药物的口服生物利用度。
据文献报道2,美国上市的药品中约50%的药物都是使用的盐型。常见的如《我不是药神》电影中的抗癌神药伊马替尼、降压药美托洛尔、止痛抗炎药双氯芬酸等等,都是通过成盐来提高的药物的溶解性。双氯芬酸是一种非甾体类抗炎药,已有多种盐型上市,包括钠盐、钾盐。在水中,游离态的双氯芬酸溶解度很低(约0.02 mg/mL),而钠盐和钾盐的溶解度分别为9.7 mg/mL、4.6 mg/mL,通过成盐,其溶解度得到了极大的提高。
2. 多晶型
多晶型现象在小分子药物中广泛存在,同一药物,由于结晶条件(如溶剂、温度、冷却速度等)和操作方式(静置挥发、搅拌、反溶剂添加等)不同,形成结晶时分子排列与晶格结构不同,因而可能形成不同的晶型,即产生多晶型。晶型不同,导致晶格能不同,药物的熔点、溶解速度、溶解度等也不同。一般来说,稳态晶型的吉布斯自由能最小、熔点高、溶解速度慢、溶解度小。因此,有些药物可以通过选择满足要求的亚稳态晶型来提高药物的溶解度。
对于多组分结晶形式,还包括溶剂合物晶型和共晶。溶剂合物晶型是药物在结晶过程中溶剂分子进入晶格使结晶型发生改变,形成药物的溶剂化物。如溶剂为水,即为水合物。在多数情况下,药物在水中的溶解度和溶解速度按水合物、无水物、有机溶剂合物的顺序依次降低。
根据FDA《Regulatory Classification of Pharmaceutical Co-Crystal(2018)》,共晶是指在同一晶格中,由两种或者两种以上不同分子按照固定的化学计量比,通过非离子键和非共价键结合形成的晶体材料。不用于盐型属于一种新的API,共晶的监管分类可以视作化合物的多晶型。共晶可以用于改善药物溶解度、生物利用度和稳定性等。
3. 减小粒径
微粉化是利用流体动力学的方法,将物料颗粒粉碎至微米级粉末的过程。经过微粉化的原料药具有更大的比表面积、孔隙率和表面能。因此,API微粉化可以改善难溶性药物的溶解度和生物利用度。微粉化技术已经成为较成熟的API工艺化的技术,目前已成功应用在临床和商业化的产品中,更适合DCSⅡa类的化合物。
另一种新型的减小粒径的方法是纳米晶,纳米晶药物是指药物颗粒的尺寸处于纳米级别,根据定义,纳米晶尺寸小于1 μm,实际应用中,通常尺寸在200-500 nm。纳米晶药物制剂通常具有非常小的粒径,这种微小的尺寸赋予了纳米晶药物一些独特的性质和优势,例如增强的药物溶解度、增加的表面积、改善的生物利用度以及更快的药物释放速度,更适合DCSⅡa类的化合物。该技术也存在一些缺点,如制备工艺复杂、控制难度大、生产成本高。
4. 无定形固体分散体
无定形固体分散体是一类较成熟、广泛应用的制剂技术,也是提高难溶性药物生物利用度最有效的策略之一。无定形固体分散体不仅可以增加药物的溶解度和溶出速度,还可以有效地减少食物效应。
无定形固体分散体的增溶原理涉及将难溶性药物以非晶态形式均匀分散在载体中,通过提高药物分散性、增加表面积、提高溶解速度,来实现药物的可溶性和生物利用度的提高。喷雾干燥和热熔挤出是两种常用的制备无定形固体分散体的方法,目前已有三十多个产品成功商业化。
5. 环糊精包合
环糊精是一类具有亲水性表面和疏水性空腔的环状寡糖,具有高度的水溶性。空腔可与疏水性溶质相结合形成包合物,从而增大溶质的表观溶解度。此外,环糊精包合还可能改变吸收部位的脂质屏障,促进药物吸收以提高生物利用度。这主要是因为环糊精可与胆固醇、磷脂和蛋白质等膜成分形成复合物,从而改变脂质屏障的通透性。
6. 添加表面活性剂
表面活性剂是同时具有极性的亲水基团和非极性的亲油基团的两亲性分子。非极性基团通常是长度在8个碳原子以上的烃链,或者是含有杂环或芳香族基团的碳链;极性基团可以是解离的离子或是不解离的亲水基团,如羧酸及其盐。
表面活性剂具有很强的表面活性,其特殊结构可以在两相界面发生定向排列从而使液体的表面张力显著下降,因此常被应用于增溶,如微乳,即由水相、油相、表面活性剂和助表面活性剂按适当比例形成的一种透明或半透明的、低粘度、各向同性且热力学稳定体系。微乳可以作为口服给药的载体,口服给药后可经淋巴吸收,从而克服了首过效应以及大分子药物通过胃肠道上皮细胞膜的障碍,使药物可以直接被机体利用,提高难溶性药物的溶解度和生物利用度。
03
常用的难溶口服药物增溶方法有多种,选择合适的方式通常需要综合考虑药物的特性、开发阶段、目标剂量、开发成本等。晶云药物拥有多晶型包括盐/共晶的筛选平台、晶型评价技术平台以及难溶性口服制剂技术平台,可为客户提供系统的难溶药物增溶的解决方案,包括盐和多晶型的筛选、API微粉化、纳米晶、无定形固体分散体技术等。如有任何口服药物增溶问题,欢迎垂询。
CRO事业部 - 专注药物晶型研发服务
18934597529(高先生)
18934597532(刘女士)
18934597535(姚女士)
collaboration@crystalpharmatech.com
CDMO事业部 - 专注制剂研发与生产服务
18015418250(王女士)
18015585433(刘女士)
18015584933(韩先生)
cfs@crystalpharmatech.com
参考资料
[1] Sandeep Kalepu et al. Insoluble drugdelivery strategies: review of recent advances and business prospects[J]. Acta Pharmaceutica Sinica B, 2015,5(5):442–453.
[2] Evan A Thackaberry. Non-clinical toxicological considerations for pharmaceutical salt selection[J]. Expert Opin Drug Metab Toxicol, 2012,8(11):1419-1433.
[3] James M. Butler et al. The Developability Classification System: Application of Biopharmaceutics Concepts to Formulation Development[J]. Journal of Pharmaceutical Sciences, 2010, 99(12): 4940-4954.
[4] Book: Nanostructures for Oral Medicine. 2017.
[5] Ron Liu. 《难溶性药物制剂技术》. 刘荣译. 北京:化学化工出版社,2021.
[6] 田阳等.纳米晶体药物制备技术的研究进展[J]. 药学学报, 2021, 56(7): 1902-1910.
[7] Pharmaceutical Co-Crystals: FDA Finalizes Guidance – RAPS.
[8] 崔德福. 《药剂学》. 人民卫生出版社,第7版.