

2023年10月10日,诺和诺德公布Semaglutide在治疗合并肾功能不全的2型糖尿病和慢性肾病的中期疗效优异,结果符合某些预先设定的标准,将提前结束临床III期。这是GLP-1受体激动剂新适应症研究,又一重大突破。
胰高血糖素样肽-1受体(GLP-1R)激动剂药物因具有优异的降糖效果、心血管保护作用及较好的减肥效果,尤其是在减肥领域巨大的市场潜力,成为了国内外许多药企争相布局的赛道。如今GLP-1R激动剂药物重磅程度和研发热情不亚于当年的PD-1/PD-L1,诺和诺德Semaglutide和礼来的Tirzepatide减肥霸主地位之争,也堪比当年的K药和O药。针对市场潜力大的靶点,新药公司常采用First in class、Best in class、Fast follow,以及明显差异化的产品开发策略。目前针对GLP-1R激动剂新药的研发已形成长效剂型,口服剂型,双/多重靶点,高药效、多适应症和小分子药物等开发策略。一场涉及药物结构、药物效果、药物剂型、给药频率的多维度竞赛正在激烈进行中。在GLP-1R激动剂巨大的市场价值和潜力吸引下,新药公司需要吸取PD-1/PD-L1的经验,如何更好的布局GLP-1药物领域并具有市场竞争力,是新药公司需要慎重思考的问题。
Tirzepatide获批,点燃双/多靶点激动剂药物开发热情
由于糖尿病、肥胖等代谢性疾病具有并发性和异质性的特点,单一靶点、单一分子的治疗疗效有限,多种药物联合使用的给药方式、临床研究相对复杂,开发多靶点的单分子激动剂便成为了糖尿病、肥胖等代谢领域的一个重要方向。研究发现,GLP-1R与其他不同的胃肠激素共同给药呈现出促进或协同作用,因而目前开发的多靶点激动剂多选择GLP-1R与其他受体联合开发。
基于药渡数据库,小编对包含GLP-1R靶点的药物进行了统计。截至2023年10月8日,除去已获批及临床终止或无进展药物,目前在研的包括GLP-1R靶点的药物(包括临床前阶段)共计173个,其中27%药物为双靶点激动剂,7%药物为多靶点激动剂,见图1。不同于GLP-1R单靶点激动剂已有多款品种获批上市,双/多靶点激动剂仅有一款获批药物,95%处于临床II期及之前阶段,见图2。
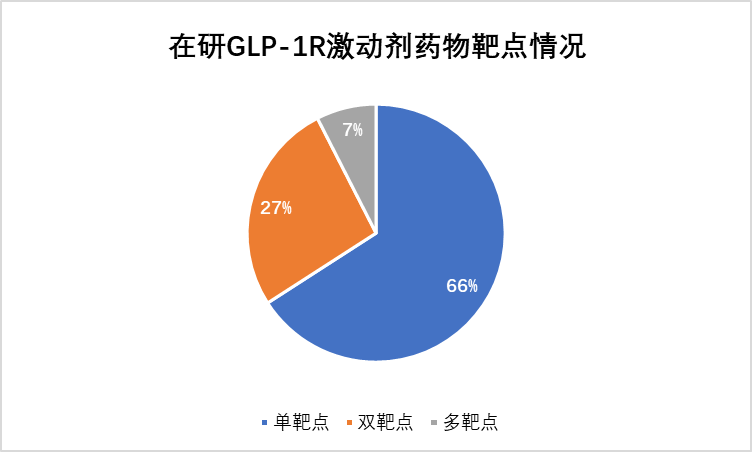
图 1
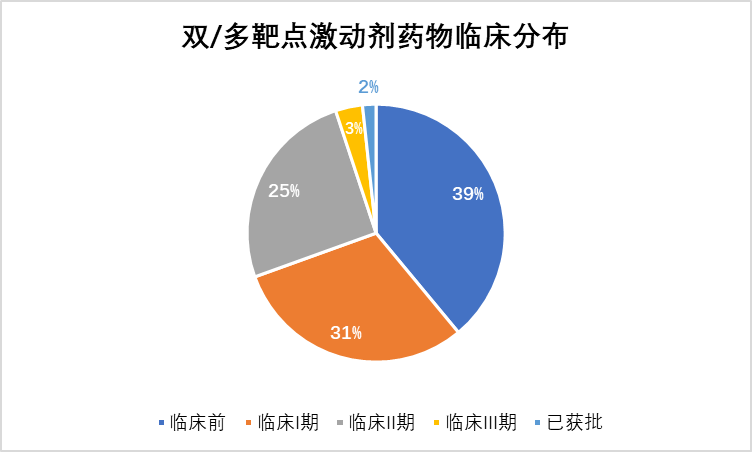
图 2
针对在研的双靶点激动剂,从GLP-1R联合的靶点类型来看,目前临床上联合比较多的靶点受体有胰高糖素(GCG)、葡萄糖依赖性促胰岛素多肽(GIP)、成纤维细胞生长因子21(FGF-21),分别占比41%、39%、9%,见图3。全球在研的双靶点激动剂大部分集中在GLP-1R/GIPR、GLP-1R/GCGR。
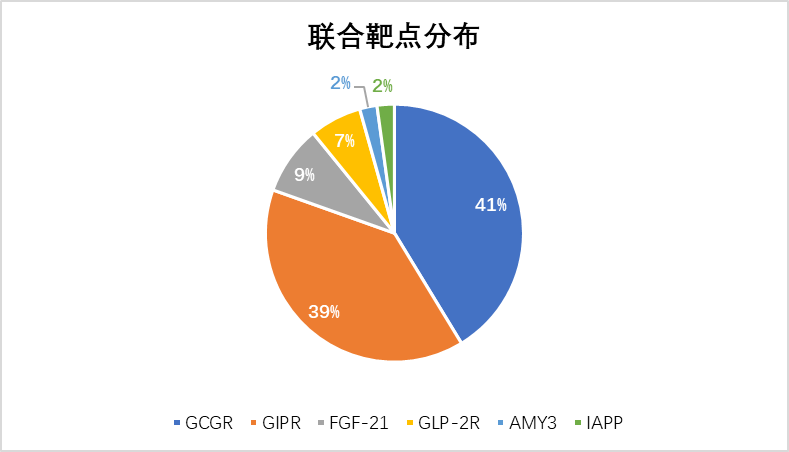
图 3
针对在研的双靶点激动剂,从临床进展来看,GLP-1R/GIPR领域由礼来的Tirzepatide领衔。Tirzepatide于2022年5月在美国获批,为每周一次注射剂,是首个且目前唯一获批的GLP-1R/GIPR激动剂药物。在代号为SURPASS-2的大型III期头对头临床中,Tirzepatide击败了Semaglutide,显示在降低血糖和减轻体重方面的效果均优于Semaglutide。基于其优异的治疗效果,Tirzepatide上市仅一年,已为礼来贡献了将近17.5亿美元的收入。该药增势迅猛,2023年上半年销售额已达15.48亿美元。礼来预计Tirzepatide 2023年总销售额将突破40亿美元。Tirzepatide优异的临床效果和销售数据,点燃了双/多靶点受体激动剂开发热情。
GLP-1R/GCGR领域由信达的Mazdutide领衔。Mazdutide为每周一次注射剂,目前正在开展治疗2型糖尿病和肥胖的III期临床。2023年5月份公布的临床II期数据显示,Mazdutide 9 mg治疗方案在平均BMI 34.3 kg/㎡的中国肥胖人群中,治疗24周后,相对于安慰剂减重幅度为15.4%(14.7 kg)。信达声称Mazdutide是全球首个在24周体重较安慰剂降幅突破15%的GLP-1R双靶点激动剂,展现出同类最优减重效果。Mazdutide有望成为首个获批上市的GLP-1R/GCGR双靶点激动剂药物。此外,还有30个双靶点激动剂在临床不同阶段。
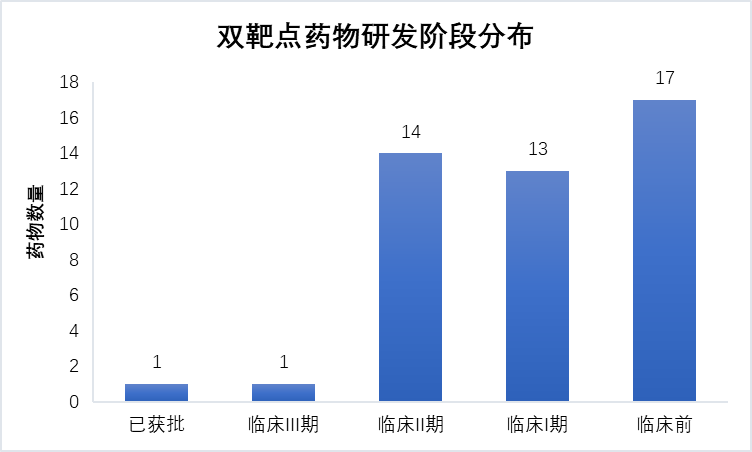
图 4
不仅是双靶点激动剂,三靶点激动剂也已表现出更强劲的疗效。礼来GLP-1R/GIPR/GCGR三靶点激动剂药物Retatrutide已成功推进III期临床,为首个进入临床III期的三靶点激动剂药物。2023年6月份公布的临床II期结果显示,治疗 24 周时,Retatrutide(1 mg、4 mg、8 mg或12 mg)在肥胖或超重(糖尿病除外)成年患者中达到疗效评估的主要终点,平均减重17.5%。在治疗48周时,接受每周注射12 mg Retatrutide治疗的受试者平均减重24.2%。此外,韩美药业已将其GLP-1R/GIPR/GCGR三靶点激动剂药物Efocipegtrutide推进至II期临床试验。另外还有5个多靶点药物推进到临床I期。
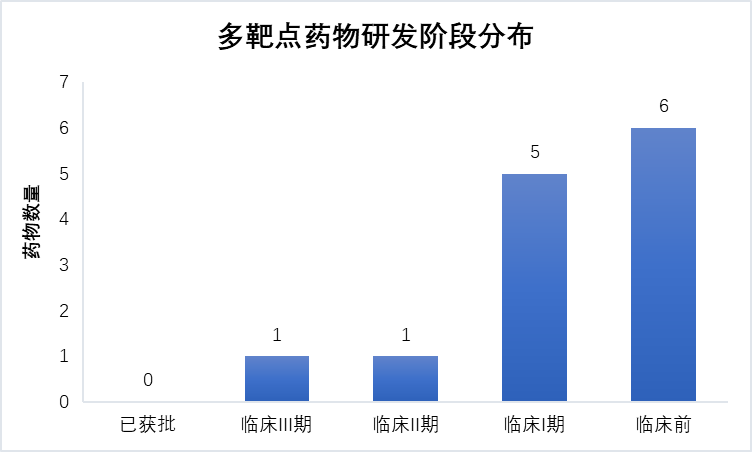
图 5
口服Semaglutide,打开多肽GLP-1R口服治疗大门
尽管GLP-1R药物已从短效迭代至长效剂型,但每周一次的注射频率仍无法给患者带来最佳的药物依从性。尤其对于糖尿病、肥胖这类需要长期用药的疾病,口服的便利性和依从性优势不言而喻。然而,目前已上市GLP-1R激动剂均为大分子多肽类似物。多肽易受胃肠道环境影响及消化酶降解,半衰期短,且多肽胃肠道黏膜穿透能力差,口服生物利用度低,这也是胰岛素暂时无法实现口服的主要原因之一。因此,若能从患者依从性上找到突破口,就意味着抓牢了竞争筹码。
2019年9月,诺和诺德的Semaglutide口服片在美国的获批,标志着口服多肽治疗的新时代的到来,也为患者带来新的用药选择。Semaglutide口服片开发历程详见控糖、减重、降低心血管风险---“潜力无限”的司美格鲁肽及其口服片剂介绍。
另辟蹊径,小分子非肽GLP-1R激动剂初露锋芒
GLP-1R激动剂类药物中多肽类居多,尽管Semaglutide口服剂型已获批,但仍存在口服生物利用度低的问题,且Semaglutide的口服制剂配方和策略并不见得适用于其他GLP-1R激动剂的多肽药物。目前已有部分企业开始绕道而行,选择开发小分子非肽类GLP-1R激动剂,进而从根源上解决生物利用度低问题。全球进展最快的小分子非肽口服GLP-1R激动剂药物为礼来的Orforglipron。2023年6月公布的临床II期结果显示,肥胖或超重的成年人接受Orforglipron治疗36周后平均减重14.7%。该药针对2型糖尿病、肥胖、心血管疾病开展了7个临床III期,其中包括和Semaglutide口服片的头对头研究,主要试验预计2025年7月完成。
多款小分子GLP-1R单靶点激动剂也紧跟其后,如辉瑞的Danuglipron,中美华东的TTP-273, 硕迪生物的GSBR-1290,上海齐鲁锐格医药的RGT-075。这些药物也均已进入临床II期。
“多靶点+口服给药”双重加码,潜力更大
在竞争激烈的GLP-1R激动剂领域,多种优势的组合相当于给药物上了多重保险,多靶点+口服剂型的组合可以作为新药公司新的方向。关于多靶点口服剂型在研品种目前公开报道的较少,小编目前仅检索到Viking Therapeutics公司的GLP-1R/GIPR双激动剂药物VK-2735,目前在临床I期,预计于2023年下半年会公布结果。此前VK-2735注射剂临床I期结果显示,28天时,VK2735组体重与基线相比下降幅度达7.8%(平均体重下降约8.2公斤)。初步来看,“多靶点+口服给药”的GLP-1R激动剂布局,对企业口服制剂的创新和技术能力提出了较高要求。尽管目前公开的竞争尚不激烈,但可以预见的是,已经在该赛道上布局多肽注射给药的企业都无法忽略对 “多靶点+口服给药”的探索,这样才能在这个巨大的赛道上建立起坚不可摧的护城河。
总结
诺和诺德和礼来在GLP-1R领域已占据大半壁江山,后入局者若想该领域占有一席之地,速度和差异化是关键。新药公司为了在激烈的竞争局面中胜出,需要打出提高药物效果、降低给药频率、改为口服剂型等组合拳,为产品竞争优势上多重保险。